CAPÍTULO 4 CÉLULAS A COMBUSTÍVEL DE HIDROGÊNIO
Células a combustível, ou Fuel Cells (FCs), são dispositivos eletroquímicos que convertem diretamente a energia química de um combustível gasoso em eletricidade, realizando o processo inversor dos eletrolisadores. Elas são vistas como potenciais fontes de energia alternativa para aplicações estacionárias e de mobilidade.
Diferentemente de uma bateria, que armazena energia e precisa ser recarregada, a célula a combustível opera continuamente, produzindo eletricidade em corrente contínua (CC), além de água e calor, desde que o combustível (como o hidrogênio) e um oxidante (como o oxigênio, geralmente do ar atmosférico) sejam constantemente fornecidos, como mostrado na Figura 4.1.
![Entradas e saídas de uma célula a combustível. Fonte: Adaptado de [19].](figura10.png)
Figura 4.1: Entradas e saídas de uma célula a combustível. Fonte: Adaptado de [19].
O princípio de operação das células a combustível, descoberto originalmente em 1839 por William R. Grove, baseia-se em uma reação eletroquímica. Os processos eletrolíticos para a geração de hidrogênio, separam a água e o hidrogênio em um eletrolisador. As células a combustível normalmente usam o processo eletrolítico inverso do eletrolisador, com diferentes tipos de eletrólito. O princípio de funcionamento de todas as células é semelhante, exceto o tipo de eletrólito [19].
Uma célula básica, como mostrado no diagrama de blocos da Figura 4.2, consiste em um eletrólito posicionado entre dois eletrodos. O eletrólito possui a propriedade especial de permitir a passagem de íons positivos (prótons), mas bloquear os elétrons. O gás hidrogênio (\(H_2\)) passa sobre o ânodo (Eletrodo de Combustível) e, com a ajuda de um catalisador (geralmente platina), separa-se em elétrons (\(e^-\)) e prótons de hidrogênio (íons positivos, \(H^+\)). Os elétrons são forçados a viajar através de um circuito elétrico externo (a carga) para chegar ao cátodo, gerando assim a corrente elétrica. Os prótons (íons) passam através do eletrólito e se combinam com os elétrons que chegam do circuito externo e com o oxigênio (geralmente do ar) para formar água (\(H_2O\)) e calor no cátodo (Eletrodo de Oxidante). Esse calor pode ser utilizado para atender as necessidades de aquecimento, incluindo água quente e aquecimento do ambiente.
![Diagrama de blocos de uma célula a combustível. Fonte: Adaptado de [19].](figura11.png)
Figura 4.2: Diagrama de blocos de uma célula a combustível. Fonte: Adaptado de [19].
Sistemas de células a combustível representam uma área industrial nova e promissora, recebendo considerável investimento comercial como uma futura tecnologia de energia. O desenvolvimento e o progresso dessa tecnologia devem ser observados de perto, pois as FCs complementam os motores a combustão e reduzem a dependência dos combustíveis fósseis. Essa tecnologia traz implicações ambientais significativas, pois o setor de transporte, por exemplo, é responsável por 32% da emissão global de \(CO_2\) [20]. A viabilidade, eficiência e robustez da tecnologia de células a combustível dependem criticamente do entendimento, previsão, monitoramento e controle do sistema.
As células a combustível são ativamente estudadas para diversas aplicações que podem ser separadas em:
Aplicações em Mobilidade (Automotivas): O uso em powertrains automotivos é enfatizado devido à sua importância no consumo global de combustível e na geração de emissões. O desempenho transiente é um requisito chave para o sucesso dos veículos a célula a combustível.
Geração de Energia Estacionária e Residencial (Geração Distribuída - GD): Fornecem energia limpa e eficiente para edifícios e residências, sendo atrativas devido à sua alta eficiência de conversão de combustível e baixíssimas emissões de gases poluentes.
4.1 Tipos de células a combustível
As células a combustível são classificadas principalmente pelo tipo de eletrólito que utilizam, sendo os tipos principais:
Células a combustível de eletrólito de membrana polimérica trocadora de prótons (Proton Exchange Membrane Fuel Cells ou Polymer Electrolyte Membrane Fuel Cells – PEMFC).
Células a combustível alcalinas (Alkaline Fuel Cells – AFC).
Células a combustível de troca aniônica (Anion Exchange Membrane Fuel Cells – AEMFC)
Células a combustível de óxido sólido (Solid Oxide Fuel Cells – SOFC).
Células a combustível de carbonatos fundidos (Molten Carbonate Fuel Cells – MCFC).
Células a combustível de ácido fosfórico (Phosphoric Acid Fuel Cells – PAFC).
A Tabela 4.1 apresenta as principais características dos tipos de célula a combustíveis mais comuns.
| Tipo | Sigla | Eletrólito | Faixa de Temperatura | Aplicações Comuns |
|---|---|---|---|---|
| Membrana de Eletrólito Polimérico Trocadora de Prótons | PEMFC | Polímero Sólido (p. ex., Nafion) | Baixa (50°C a 100°C) | Automotiva, residencial, portátil. |
| Alcalina | AFC | Hidróxido de Potássio Líquido | Baixa (60°C a 90°C) | Espaço (transporte inicial). |
| Membrana de Eletrólito Polimérico Condutora de Ânions | AEMFC | Polímero sólido | Baixa (60°C a 80°C) | Ainda em desenvolvimento. |
| Óxido Sólido | SOFC | Cerâmica Sólida | Alta (600°C a 1000°C) | Geração estacionária, cogeração de calor e energia. |
| Carbonato Fundido | MCFC | Carbonato Fundido | Alta (600°C a 700°C) | Geração estacionária, cogeração de calor e energia. |
| Ácido Fosfórico | PAFC | Ácido Fosfórico Líquido | Média(150°C a 220°C) | Geração estacionária, dispersa. |
4.2 A estrutura da célula a combustível e seus componentes
Uma única célula a combustível tipicamente produz uma tensão baixa de cerca de 0,4 V a 0,9 V e correntes elevadas entre 0,5 a 1,0 A/cm2. Para produzir a tensão e potência necessárias para a maioria das aplicações, múltiplas células são conectadas em série, formando um Stack, como mostrado na Figura 4.3.
Os componentes básicos de uma célula individual são:
Conjunto Membrana Eletrodo (do inglês, Membrane Electrode Assembly – MEA): Consiste na membrana (eletrólito polimérico no caso da célula PEM, por exemplo), os eletrodos (ânodo e cátodo) e as camadas de difusão de gás. O catalisador (geralmente platina na célula PEM) é aplicado à superfície do ânodo e do cátodo para acelerar a reação.
Placas bipolares (em inglês, Flow Field Plates): Distribuem os gases reagentes através de canais de fluxo, coletam a corrente produzida pela reação eletroquímica e fornecem suporte estrutural.
![Esquemático da operação e componentes de um stack de célula a combustível. Fonte: [21].](figura12.png)
Figura 4.3: Esquemático da operação e componentes de um stack de célula a combustível. Fonte: [21].
A Figura 4.4 mostra um exemplo de um stack de célula a combustível comercial.
![Exemplo de um stack de célula a combustível tipo PEM. Fonte: [22].](figura13.png)
Figura 4.4: Exemplo de um stack de célula a combustível tipo PEM. Fonte: [22].
Várias células a combustível podem ser ligadas em série e paralelo para aumentar a capacidade de potência de saída, como mostra o diagrama de blocos da Figura 4.5 [23] [24]. Um inversor PWM (Pulse Width Modulation) é muitas vezes empregado para produzir uma tensão alternada (CA) fixa ou variável, com uma frequência também fixa ou variável. Normalmente, utiliza-se um transformador antes de se conectar o inversor à rede elétrica. Em um sistema híbrido de célula a combustível, outras fontes de energia, como baterias e supercapacitores, também podem ser integradas para aumentar ainda mais a eficiência e a estabilidade do sistema.
![Diagrama de blocos de um sistema de células a combustível conectado à rede elétrica. Fonte: Adaptado de [19].](figura14.png)
Figura 4.5: Diagrama de blocos de um sistema de células a combustível conectado à rede elétrica. Fonte: Adaptado de [19].
4.3 Células a combustível de baixa temperatura
Como apresentado na seção 4.1, as células a combustível (FCs) são comumente classificadas com base no tipo de eletrólito utilizado, o que determina suas características operacionais, como a temperatura de operação. As células podem ser divididas em dois grupos principais: células de baixa temperatura e células de alta temperatura.
As principais células a combustível de baixa temperatura são as células de eletrólito de membrana polimérica trocadora de prótons (PEMFC) e as células alcalinas (AFC). As células de membrana de troca aniônica (AEMFC) estão em desenvolvimento e tem ganhado atenção nos últimos anos. A seguir será detalhado o funcionamento de cada umas destas células.
4.3.1 Células a combustível de eletrólito de membrana polimérica de troca de prótons (PEMFC)
A PEMFC é a principal tecnologia atual entre as células de baixa temperatura devido a sua alta densidade de potência, eletrólito sólido e faixa de temperatura de operação (50°C a 100°C), sendo adequadas para aplicações automotivas e sistemas de geração distribuída de pequeno e médio porte. A baixa temperatura permite uma partida rápida, no entanto, o gerenciamento térmico é desafiador, pois a temperatura deve ser mantida abaixo de 100°C para que a membrana permaneça adequadamente umidificada. A membrana de polímero é um excelente condutor de íons de hidrogênio.
Os componentes básicos da célula a combustível PEM são o anodo, o eletrólito e catodo, como indica a Figura 4.6.
![Esquemático de uma célula a combustível PEM. Fonte: Adaptado de [19].](figura15.png)
Figura 4.6: Esquemático de uma célula a combustível PEM. Fonte: Adaptado de [19].
O eletrólito é uma membrana de polímero revestido por um catalisador de metal, como a platina. O anodo tem uma placa plana com canais embutidos para dispersar o gás hidrogênio sobre a superfície do catalisador. Quando o hidrogênio pressurizado entra no anodo e em seguida passa pelo canal, o catalisador faz dois átomos do gás hidrogênio (\(2H_2\)) se oxidarem em quatro íons de hidrogênio (\(4H^+\)) e abandonarem 4 elétrons (\(4H^+\)). A reação no anodo pode ser representada pela equação química (4.1).
\[\begin{equation} 2H_2 \rightarrow 4H^+ + 4e^- \tag{4.1} \end{equation}\]
Os elétrons livres fluem pelo caminho de menor resistência da carga externa para o outro eletrodo (cátodo). A corrente de carga é causada pelo fluxo de elétrons. A direção do fluxo de corrente consiste no sentido oposto do fluxo de elétrons. Os íons de hidrogênio passam através da membrana do anodo para o catodo. Ao entrar no catodo, os elétrons reagem com o oxigênio do ar exterior e os íons de hidrogênio do catodo formando água. A reação catódica pode ser representada pela equação (4.2). Todo esse processo está representado na Figura 4.6.
\[\begin{equation} O_2 + 4H^+ + 4e^- \rightarrow 2H_2O \tag{4.2} \end{equation}\]
Portanto, a célula a combustível PEM combina hidrogênio com oxigênio para produzir água, e isso gera energia térmica no processo de reação do catodo. A energia térmica pode ser extraída por meio de um trocador de calor, como na Figura 4.2, para uso em várias aplicações. A reação geral do anodo e catodo pode ser representada pela equação química dada em (4.3).
\[\begin{equation} 2H_2 + O_2 \rightarrow 2H_2O + \text{energia (calor)} \tag{4.3} \end{equation}\]
Uma célula a combustível PEM funciona a temperaturas relativamente baixas, de cerca de 80°C, e pode variar rapidamente a sua saída para atender às mudanças na demanda de energia (com resposta a um degrau de carga em centenas de milissegundos) [23]. O dispositivo é de certa forma leve, possui alta densidade de energia e pode iniciar a operação muito rapidamente (em alguns segundos). Essa célula é adequada para muitas aplicações, incluindo o transporte e a distribuição para cargas residenciais. Por exemplo, uma célula a combustível PEM equipa o Toyota Mirai, o primeiro carro a hidrogênio a ser produzido em massa e vendido comercialmente no mundo.
Entretanto, a platina utilizada como catalisador é extremamente sensível ao monóxido de carbono, e a eliminação deste é crucial para a longevidade da célula a combustível. Isso se soma ao custo geral do sistema PEM. A execução na prática requer unidades de controle, como o regulador de pressão do hidrogênio, como ilustra a Figura 4.2, e um controle do fluxo de ar (ou de \(O_2\)).
A célula a combustível com membrana polimérica de troca de prótons (PEMFC) emprega camadas de catalisador revestidas em ambos os lados de uma membrana polimérica para catalisar as reações no catodo e no anodo, conforme Figura 4.6.
Na maioria dos projetos, o catalisador é baseado em platina, um metal precioso muito caro. A platina pode contribuir com 10% a 15% do custo de um stack de células a combustível. A menos que o teor de platina seja reduzido, ele representará uma parcela maior do custo à medida que os volumes de fabricação aumentam. Muitos pesquisadores estão se concentrando em encontrar substitutos mais baratos e duráveis para a platina, mesmo que ainda não apresentem um desempenho comparável ao da platina. Atualmente, catalisadores à base de ligas de platina (com menor teor de platina) e catalisadores não baseados em platina (utilizando metais não preciosos) são substitutos promissores. Diferentes tipos catalisadores com nanoestruturas tipo Core-shell, nanocristais e outras estão em desenvolvimento [25]. Contudo, ainda há um longo caminho a percorrer antes que eles possam ser empregados na fabricação prática e aplicações industriais, como mostrado na Figura 4.7.
![Linha do tempo para tecnologia dos catalisadores de Platina, liga de Platina, core-shell, metais não preciosos, nanocristais com forma controlada e nanoestrutura. Fonte: Adaptado de [25].](figura16.png)
Figura 4.7: Linha do tempo para tecnologia dos catalisadores de Platina, liga de Platina, core-shell, metais não preciosos, nanocristais com forma controlada e nanoestrutura. Fonte: Adaptado de [25].
4.3.2 Células a combustível alcalinas (AFC)
As células a combustível alcalinas utilizam um eletrólito alcalino como o hidróxido de potássio (\(KOH\)) ou uma membrana alcalina. A célula a combustível alcalina funciona a temperaturas elevadas, de 65°C a 220°C; portanto, tem partida mais lenta em relação à célula PEM. Os principais componentes da célula a combustível alcalina são mostrados na Figura 4.8.
![Diagrama de blocos de uma célula a combustível alcalina. Fonte: Adaptado de [19].](figura17.png)
Figura 4.8: Diagrama de blocos de uma célula a combustível alcalina. Fonte: Adaptado de [19].
O hidrogênio reage no anodo com os íons de hidroxila \(OH^-\) do KOH para produzir água e quatro elétrons livres (\(4e^-\)). A reação no anodo pode ser representada pela equação química (4.4).
\[\begin{equation} 2H_2 + 4OH^- \rightarrow 4H_2O + 4e^- \tag{4.4} \end{equation}\]
A água produzida no anodo retorna para o catodo. Os íons hidroxila são gerados no catodo pela combinação de oxigênio, água e elétrons livres. A reação do anodo pode ser representada pela equação química (4.5).
\[\begin{equation} O_2 + 2H_2O + 4e^- \rightarrow 4OH^- \tag{4.5} \end{equation}\]
A reação geral de anodo e catodo pode ser representada pela equação química (4.6).
\[\begin{equation} 2H_2 + O_2 \rightarrow 2H_2O + \text{energia (calor)} \tag{4.6} \end{equation}\]
A célula a combustível alcalina é muito suscetível à contaminação, em especial pelo dióxido de carbono (\(CO_2\)), que reage com o eletrólito e rapidamente degrada o desempenho da célula a combustível. A água e o metano também podem contaminar a célula a combustível. Portanto, a célula a combustível alcalina deve funcionar com hidrogênio e oxigênio puros, o que aumenta o custo de sua operação. Assim, a aplicação da célula a combustível alcalina fica limitada a ambientes controlados, como naves espaciais. A NASA utilizou células a combustível alcalinas em missões espaciais e agora está encontrando novas aplicações para ela, como em energia portátil.
4.3.3 Célula a combustível de membrana de troca aniônica (AEMFC)
Outras tecnologias vêm se desenvolvendo como alternativa ao elevado custo da célula a combustível PEM e uma delas é a célula a combustível de membrana de troca aniônica (AEMFC) [26]. A membrana de troca aniônica é um tipo de membrana polimérica que permite a passagem de ânions (íons negativos, como a hidroxila, \(OH^-\)) em vez de prótons (\(H^+\), como na membrana utilizada na PEM). Essa célula é uma variação da célula a combustível alcalina que utiliza um eletrólito sólido (a membrana de troca aniônica) no lugar de um eletrólito líquido, como mostrado na Figura 4.9. As características da célula a combustível de membrana de troca aniônica possibilitam o uso de catalisadores sem metais nobre, utilizando níquel, ou compostos de prata e cobalto.
![Célula a combustível de membrana de troca aniônica (AEMFC). Fonte: Adaptado de [19].](figura18.png)
Figura 4.9: Célula a combustível de membrana de troca aniônica (AEMFC). Fonte: Adaptado de [19].
4.4 Células a combustível de alta temperatura
4.4.1 Células a combustível de óxido sólido (SOFC)
As SOFCs se destacam entre as células que operam em temperaturas elevadas, o que lhes confere alta eficiência (até 60%) e flexibilidade de combustível (podem reformar o combustível internamente). O calor residual dessas células de alta temperatura é valioso para sistemas de Cogeração de Calor e Energia (CHP, do inglês Combined Heat and Power), alcançando eficiências globais de 75-80%.
O eletrólito da célula a combustível de óxido sólido é uma fina camada de material cerâmico duro, como o óxido de zircônio. Os principais componentes da célula a combustível de óxido sólido são mostrados na Figura 4.10.
![Diagrama de blocos de uma célula a combustível de óxido sólido. Fonte: Adaptado de [19].](figura19.png)
Figura 4.10: Diagrama de blocos de uma célula a combustível de óxido sólido. Fonte: Adaptado de [19].
As moléculas de oxigênio do ar se combinam com quatro elétrons no catodo para produzir íons de oxigênio negativamente carregados, \(O^{2-}\). Esses íons de oxigênio migram para o anodo através do material cerâmico sólido e se combinam com o hidrogênio para produzir água e quatro elétrons (\(4e^-\)). Os elétrons livres nos íons de oxigênio são liberados e passam através da carga elétrica para o catodo. A reação química no anodo é dada por (4.7).
\[\begin{equation} 2H_2 + O^{2-} \rightarrow 2H_2O + 4e^- \tag{4.7} \end{equation}\]
A reação química no catodo é dada por (4.8).
\[\begin{equation} O_2 + 4e^- \rightarrow 2O^{2-} \tag{4.8} \end{equation}\]
Então, a reação geral é dada por (4.9).
\[\begin{equation} 2H_2 + O_2 \rightarrow 2H_2O + \text{energia (calor)} \tag{4.9} \end{equation}\]
As células a combustível de óxido sólido funcionam a temperaturas muito altas, entre 600°C a 1000°C. Elas necessitam de um tempo significativo para atingir o estado estacionário, portanto, são lentas na partida e para responder às mudanças na demanda de energia elétrica. No entanto, a alta temperatura torna a célula a combustível de óxido sólido menos sensível a impurezas no combustível, como enxofre e \(CO_2\). Essas células a combustível conseguem reformar internamente o gás natural e o biogás, e podem ser combinadas com uma turbina a gás para produzir eletricidade com uma eficiência que chega a 75%. Portanto, a célula a combustível de óxido sólido é adequada para a geração estacionária de grande escala na faixa de megawatts.
4.4.2 Células a combustível de carbonato fundido (MCFC)
As células a combustível de carbonato fundido utilizam um sal de carbonato imobilizado em uma matriz porosa como seu eletrólito. O eletrólito é uma mistura de carbonado de lítio e carbonato de potássio, ou de lítio e de sódio. Os principais componentes da célula a combustível de carbonato fundido são mostrados na Figura 4.11.
![Diagrama de blocos de uma célula a combustível de carbonato fundido. Fonte: Adaptado de [19].](figura20.png)
Figura 4.11: Diagrama de blocos de uma célula a combustível de carbonato fundido. Fonte: Adaptado de [19].
As células a combustível de carbonato fundido já são utilizadas em várias aplicações estacionárias de médio a grande porte, em virtude da sua eficiência. Seu funcionamento a temperaturas elevadas, de aproximadamente 600°C, lhe permite reformar internamente combustíveis como gás natural e biogás.
Quando o eletrólito da célula a combustível de carbonato fundido é aquecido a uma temperatura em torno de 600 °C, a mistura de sal se funde e torna-se condutora para íons de carbonato \(CO_3^{2-}\). Esses íons carregados negativamente fluem através do catodo para o anodo, onde se combinam com o hidrogênio para produzir água, dióxido de carbono e elétrons livres. A reação química no ânodo é dada pela equação (4.10).
\[\begin{equation} 2CO_3^{2-} + 2H_2 \rightarrow 2H_2O + 2CO_2 + 4e^- \tag{4.10} \end{equation}\]
O dióxido de carbono é realimentado para o cátodo, onde reage com o oxigênio e os elétrons livres (\(4e^-\)). A reação química no catodo é dada pela equação (4.11).
\[\begin{equation} 2CO_2 + O_2 + 4e^- \rightarrow 2CO_3^{2-} \tag{4.11} \end{equation}\]
A reação geral da célula de carbonato fundido é dada por (4.12).
\[\begin{equation} 2H_2 + O_2 \rightarrow 2H_2O + \text{energia (calor)} \tag{4.12} \end{equation}\]
Podemos observar a partir das equações (4.10) e (4.11) que o \(CO_2\) produzido no ânodo também é consumido no cátodo, em condições ideais. Com um projeto cuidadoso, o dióxido de carbono pode ser totalmente utilizado e a célula não emite \(CO_2\). Uma das desvantagens características dessa célula é a corrosão interna por conta do eletrólito de carbonato.
4.5 Modelo equivalente de uma célula a combustível
De forma geral, a modelagem de células a combustível é muito similar a dos eletrolisadores e também apresenta alta não linearidade, sendo governada por parâmetros complexos como a densidade de corrente, a umidade da membrana (especialmente em células PEM) e as pressões parciais dos gases reagentes. Simplificações do modelo completo podem ser aplicadas conforme o foco e a profundidade do estudo em questão.
O desempenho de uma célula é tradicionalmente caracterizado pela curva de polarização, um gráfico da tensão da célula versus a densidade de corrente (corrente por unidade de área ativa), como o da Figura 4.12. A tensão de saída real da célula é sempre menor que a tensão ideal, devido as perdas. À medida que mais corrente é extraída da célula, a tensão diminui.
![Curva característica de uma célula a combustível mostrando as diferentes regiões de operação. Fonte: [27].](figura21.png)
Figura 4.12: Curva característica de uma célula a combustível mostrando as diferentes regiões de operação. Fonte: [27].
As três principais categorias de perdas são:
Perda por Ativação (\(\eta_{act}\)): A tensão cai em baixas correntes. É devida à barreira de energia que as espécies reagentes devem superar para iniciar a reação química no eletrodo.
Perda Ôhmica (\(\eta_{ohm}\)): Ocorre na faixa média da curva, sendo aproximadamente linear com a corrente. É causada pela resistência elétrica dos componentes, como o eletrólito e os eletrodos.
Perda de Concentração (\(\eta_{conc}\)): Ocorre em altas correntes. É causada pelo transporte lento e ineficiente dos gases reagentes (hidrogênio e oxigênio) para os locais da reação, levando a uma queda acentuada na tensão de saída. A operação nesta zona extrema deve ser evitada para preservar a integridade da célula.
Assim, a tensão da célula pode ser dada pela equação (4.13)
\[\begin{equation} E_{cel} = E_{rev} - \eta_{act} - \eta_{ohm} - \eta_{conc} \tag{4.13} \end{equation}\]
A tensão reversível \(E_{rev}\) é descrita pela equação de Nernst (2.11), assim como da célula de eletrólise. Como a Equação de Nernst depende apenas da estequiometria da reação global (a oxidação do hidrogênio e redução do oxigênio para formar água: \(2H_2 + O_2 \rightarrow 2H_2O\)) e das condições operacionais (T, pressões/concentrações), ela pode ser aplicada a diversos tipos de célula. O que muda na prática para a aplicação da equação é:
Temperatura: cada tipo de célula opera em uma faixa de temperatura diferente (PEMFC: baixa; SOFC: alta), logo, o valor de T na equação mudará.
Reação química: para as células a combustível a hidrogênio puro, a reação global é a mesma, mas em células que usam combustíveis diferentes (como metanol ou gás natural) ou eletrólitos diferentes (como a MCFC), a reação do eletrodo (e, portanto, os valores de \(E_0\), \(z\) e o quociente de pressões parciais dos reagentes) é específica.
4.6 Balanço da planta de uma célula a combustível
O desempenho de uma planta de célula a combustível não depende apenas do stack eletroquímico, mas sobretudo do conjunto de subsistemas auxiliares, denominado Balanço de Planta (Balance of Plant – BoP). É esse arranjo de componentes que garante condições adequadas de operação em termos de temperatura, pressão, umidade, pureza dos gases e segurança, além de realizar a conversão da energia elétrica gerada em formas utilizáveis pela carga ou pela rede. A Figura 4.13 apresenta o exemplo de um arranjo de uma planta de uma célula a combustível.
![Arranjo de uma planta PEMFC. Fonte [28].](figura22.png)
Figura 4.13: Arranjo de uma planta PEMFC. Fonte [28].
Estudos recentes demonstram que, em diversas arquiteturas de células a combustível, o BoP pode representar mais de 50% do custo total do sistema, bem como responder por perdas parasitas significativas, que reduzem a eficiência líquida. Dessa forma, compreender a composição e as especificidades do BoP em diferentes tecnologias é fundamental para avaliar a viabilidade técnica e econômica da geração eletroquímica de energia.
Embora existam diferenças relevantes entre células de baixa e alta temperatura, o BoP segue uma lógica funcional comum: preparação e fornecimento do combustível, condicionamento do oxidante, gerenciamento térmico e de água, eletrônica de potência, além de controle e segurança. No caso das tecnologias de baixa temperatura (PEMFC, AFC e PAFC), predominam subsistemas voltados à gestão hídrica e de pureza do hidrogênio, enquanto em sistemas de alta temperatura (MCFC e SOFC) a complexidade recai sobre resistência de materiais, estabilidade térmica e integração com reformadores.
Desta forma, o BoP constitui a espinha dorsal de uma planta de célula a combustível, determinando não apenas a eficiência e a durabilidade, mas também a viabilidade econômica e de mercado. Tanto nas tecnologias de baixa temperatura quanto nos sistemas de alta temperatura a busca por soluções mais simples, robustas e de menor custo no BoP representa um dos caminhos mais promissores para a consolidação comercial das células a combustível em escala global.
A evolução do BoP busca reduzir consumo parasita, sobretudo em compressores e bombas, que impactam diretamente a eficiência líquida. Também há esforços para miniaturizar sistemas de humidificação e resfriamento em PEMFCs, reduzir a contaminação por CO₂ em AFCs e aumentar a durabilidade de materiais resistentes à corrosão e altas temperaturas em MCFCs e SOFCs. Avanços recentes apontam para a integração de modelagem preditiva e controle inteligente, capazes de prolongar a vida útil e otimizar a resposta dinâmica do sistema. Além disso, há tendência de desenvolver BoPs modulares e compactos, visando aplicações veiculares e portáteis, sem sacrificar confiabilidade.
Esses avanços no BoP refletem não apenas melhorias na eficiência energética e na durabilidade dos componentes, mas também estabelecem a base para a gestão eficiente dos subsistemas que garantem o fornecimento de combustível, oxidante, água, calor e energia elétrica. A seguir, são detalhados os principais subsistemas do BoP de um PEMFC, com suas exigências e particularidades.
Sistema de Combustível: O sistema de combustível é um dos elementos centrais do BoP. Nas PEMFCs, a exigência de hidrogênio com altíssima pureza (tipicamente > 99,99%), condição fundamental para evitar a degradação do catalisador de platina e a redução da condutividade da membrana. Para garantir esse requisito, o BoP inclui o uso de tanques de armazenamento pressurizado, válvulas de regulagem, sensores de vazamento e, em alguns casos, purificadores adicionais. Quando o combustível é obtido por meio de reformadores de gás natural ou etanol, o subsistema deve incorporar etapas de remoção de monóxido de carbono e outros contaminantes, uma vez que traços acima de 10 ppm já são suficientes para envenenar o catalisador. Além disso, a gestão adequada da pressão e da vazão de hidrogênio é essencial para evitar gradientes de concentração e garantir a uniformidade de operação das células. Em sistemas de maior porte, também se empregam linhas redundantes de alimentação, válvulas de segurança e sistemas automatizados de purga, que têm a função de remover gases inertes acumulados e manter a estabilidade eletroquímica do conjunto [29].
Fornecimento de Oxidante: O fornecimento de ar ao cátodo é um subsistema essencial no BoP das PEMFCs, sendo responsável por garantir a disponibilidade adequada de oxigênio para a reação eletroquímica. Em geral, empregam-se compressores para alimentar o ar em pressão controlada, além de filtros para remover particulados e contaminantes que possam comprometer a durabilidade da membrana [30]. Um aspecto crítico é a umidificação do ar de entrada, necessária para manter o equilíbrio hídrico da membrana polimérica, cuja condutividade iônica depende fortemente do teor de água. A insuficiência de umidade pode levar à desidratação e aumento da resistência ôhmica, enquanto o excesso pode causar alagamento dos canais de fluxo, reduzindo a eficiência da célula. Assim, o subsistema de fornecimento de oxidante deve ser integrado a estratégias de controle que equilibrem pressão, vazão e umidade, garantindo desempenho estável e prolongando a vida útil do sistema. Alguns dos elementos do sistema de fornecimento de oxidante são mostrados na Figura 4.14.
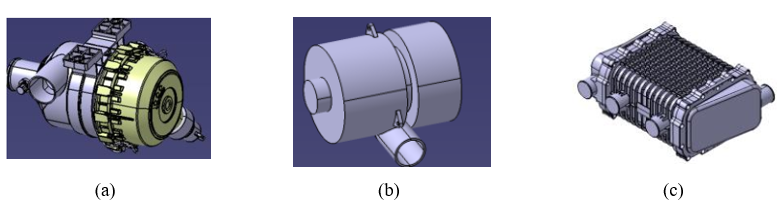
Figura 4.14: Componentes do Sistema de fornecimento de oxidante: (a) filtro de ar, (b) compressor de ar e (c) humidificador.
- Gestão Térmica e de Água: O gerenciamento térmico é um dos pontos mais críticos do BoP em sistemas de PEMFCs, já que essas células operam em baixas temperaturas (tipicamente entre 60 – 90 °C) e dependem fortemente da estabilidade térmica para manter o desempenho eletroquímico. O calor gerado durante as reações deve ser dissipado de forma eficiente, evitando elevação excessiva da temperatura, que pode degradar a membrana polimérica e acelerar a perda de desempenho do catalisador. Para isso, recorre-se normalmente ao resfriamento líquido, com bombas de circulação, trocadores de calor e radiadores, que permitem manter a temperatura do conjunto em níveis seguros e homogêneos. A Figura 4.15 mostra alguns desses componentes. Outro aspecto fundamental está no balanço de água. Durante a operação, a PEMFC consome água na região do ânodo, transporta parte dela pela membrana por eletro-osmose e ainda produz água no cátodo como subproduto da reação. Esse ciclo torna a gestão hídrica um desafio permanente: pouca água leva à desidratação da membrana e perda de condutividade iônica, enquanto o excesso provoca alagamento (flooding) nos canais de fluxo, reduzindo a difusão de reagentes. Assim, o BoP incorpora umidificadores, sistemas de recirculação e drenagem controlada, que asseguram o equilíbrio entre hidratação e remoção do excesso. Por fim, o gerenciamento integrado de calor e água deve ser apoiado por sensores e estratégias de controle em tempo real, capazes de ajustar a vazão de refrigerante e o nível de umidificação conforme a demanda elétrica. Esse equilíbrio é essencial para garantir não apenas a eficiência e a estabilidade de curto prazo, mas também a durabilidade do sistema em longas horas de operação. Quando bem implementada, a gestão térmica e hídrica amplia a vida útil da célula, reduz perdas de desempenho e contribui para a confiabilidade da planta [30] [31].

Figura 4.15: Componentes do sistema térmico e de água: (a) radiador e (b) bomba de água.
- Eletrônica de Potência: Nas células a combustível, a eletrônica de potência é um componente indispensável do BoP, pois atua como interface entre a energia elétrica gerada pelo stack e a carga externa. A célula fornece corrente contínua em tensão relativamente baixa e variável, em função da carga aplicada e do estado operacional da pilha. Para adequar essa energia ao uso final, o sistema utiliza conversores CC-CC, que estabilizam e elevam a tensão, e inversores CC-CA, quando é necessária a integração com redes elétricas convencionais ou alimentar uma carga CA. Essa conversão é essencial para garantir a compatibilidade com diferentes aplicações, desde sistemas estacionários de geração distribuída até aplicações móveis e veiculares. A Figura 4.16 monstra os circuitos utilizados na conversão CC-CC (conversor elevador) e na conversão CC-CA (conversor em trifásico em ponte H). Em aplicações automotivas, a eletrônica de potência tem papel ainda mais crítico, já que deve lidar com variações rápidas de demanda de energia. Para amortecer picos de carga e proteger o stack contra transientes elétricos, são integrados ao sistema dispositivos de armazenamento, como baterias de íons de lítio ou supercapacitores, que fornecem ou absorvem energia instantaneamente. Essa configuração híbrida não apenas prolonga a vida útil da célula ao evitar sobrecargas, como também melhora a eficiência global da planta, ao permitir que a PEMFC opere próxima a uma faixa de potência mais estável. Além disso, a eletrônica de potência possibilita a implementação de estratégias de controle avançadas, como o rastreamento do ponto de máxima potência (MPPT), que otimiza a extração de energia em condições variáveis de operação. Esse tipo de gerenciamento é fundamental para explorar a flexibilidade das PEMFCs, garantindo desempenho confiável tanto em regime estacionário quanto em cenários dinâmicos de demanda [31].
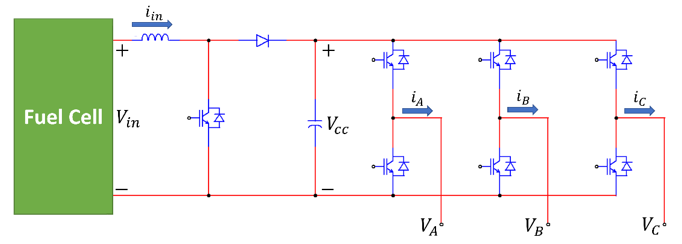
Figura 4.16: Circuitos de um conversor elevador (boost converter) para o estágio CC-CC e conversor trifásico em ponte H para o estágio CC-CA.
- Controle e Segurança: O BoP das células a combustível de membrana de troca protônica (PEMFCs) integra sistemas avançados de controle e segurança, essenciais para a operação eficiente e segura do sistema. Sensores de pressão, temperatura, vazão e umidade monitoram continuamente as condições da célula, alimentando algoritmos de controle implementados em Controladores Lógicos Programáveis (PLC) ou unidades eletrônicas de controle (ECU). Esses sistemas ajustam automaticamente os fluxos de combustível e oxidante, o gerenciamento térmico e as estratégias de umidificação, garantindo operação dentro das condições seguras e otimizando o desempenho eletroquímico. A segurança em PEMFCs é reforçada por dispositivos como válvulas de alívio de pressão, sensores de detecção de hidrogênio e protocolos de desligamento emergencial. Estes elementos protegem tanto os operadores quanto os componentes do sistema, evitando acidentes em caso de falhas, vazamentos ou sobrepressão. Em particular, a operação com hidrogênio pressurizado exige atenção especial para evitar risco de explosão ou envenenamento do catalisador por contaminantes. Além disso, a integração de algoritmos de controle avançados permite a antecipação de transientes de carga e condições de operação fora do ponto ótimo, promovendo respostas rápidas do sistema sem comprometer a integridade do stack. Essa abordagem aumenta a confiabilidade do sistema e prolonga a vida útil da PEMFC, ao mesmo tempo em que mantém a eficiência energética do conjunto [32].